01 有効性
スイニー錠は1日2回投与により、朝食後及び夕食後の活性型GLP-1を増加させ、グルカゴンを抑制することにより24時間にわたり血糖コントロールを改善する。
活性型GLP-1濃度(投与3日間)※
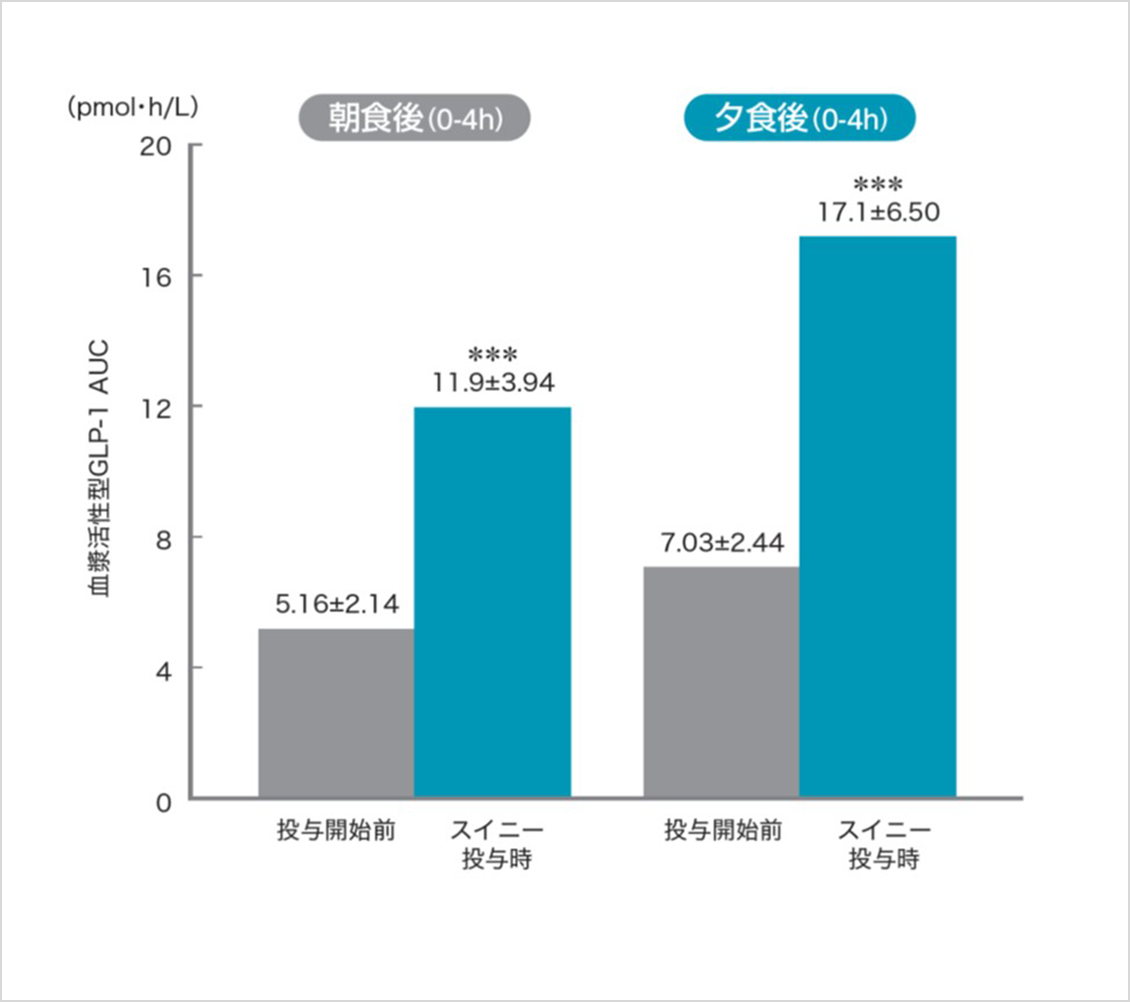
※活性型GLP-1は、固相抽出による前処理を行って測定した。
血漿グルカゴン濃度(投与3日間)
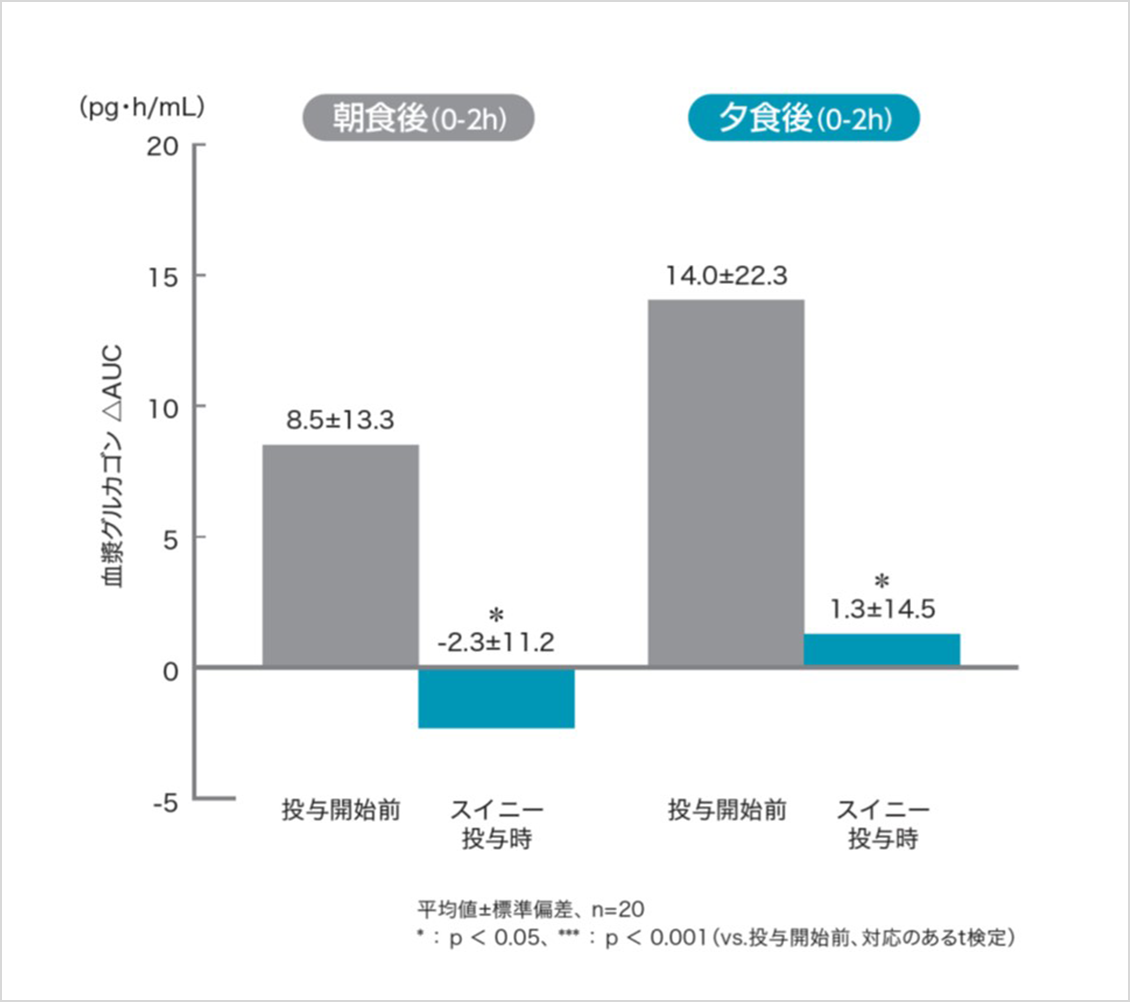
血糖値の24時間推移(CGM、投与3日目)
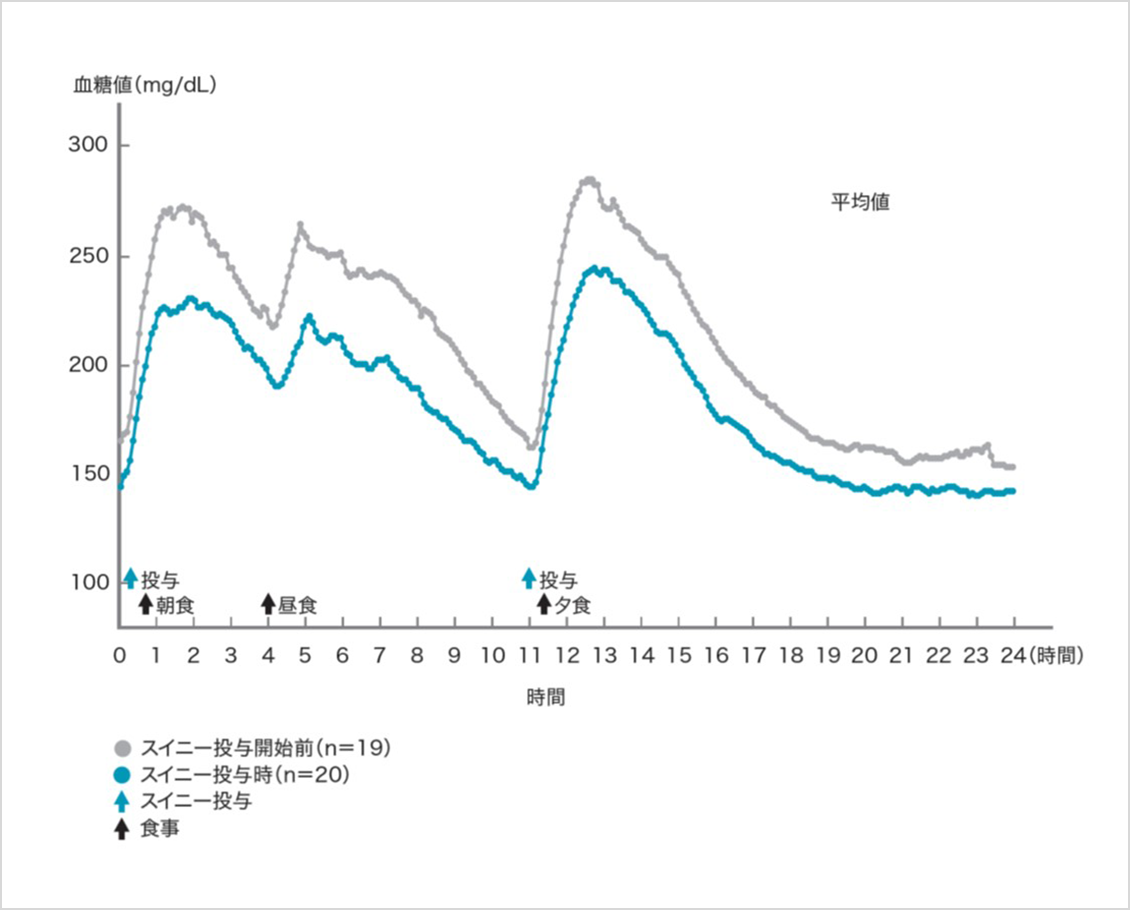
| スイニー投与開始前 (n=16) |
スイニー投与時 (n=18) |
変化量 (n=14) |
|
|---|---|---|---|
| AUCo-24h (mg.h/dL) |
4,906.0±924.9 | 4,421.9±1187.0 | -727.3±470.9*** |
| 24時間平均血糖 (mg/dL) |
204.25±38.53 | 184.10±49.39 | -30.27±19.61*** |
| M値 | 39.54±26.27 | 29.40±32.70 | -17.30±10.96*** |
| MAGE (mg/dL) |
126.50±19.03 | 104.97±32.71 | -24.38±18.59*** |
M値:Morbus値(血糖値の変動を表す指標)
MAGE:mean amplitude of glycemic excursion(血糖値の変動を表す指標)
平均値±標準偏差
:p<0.001 (vs. スイニー投与開始前)
対応のあるt検定
試験概要
- 試験名
- 臨床薬理試験
- 目的
- 対象患者におけるスイニーの薬力学的検討を行う。
- 対象
- 食事療法又は食事療法・運動療法で血糖コントロールが不十分な2型糖尿病患者(HbA1c:6.9%以上10.5%未満、年齢:20歳以上70歳未満)20例
- 方法
- 非盲検2期クロスオーバー試験。無処置期間(コントロール期)の後、スイニー100mgを1日2回(朝夕食直前)、3日間反復経口投与した。
- 評価項目
- 持続血糖測定(CGM)を用いた血糖の24時間プロファイル、薬力学的効果
※株式会社三和化学研究所 社内資料:2型糖尿病患者における薬力学的検討
02 安全性
特定使用成績調査 最終報告(3年)
安全解析対象例6,324例中の副作用発現率は9.49%であり、主な副作用は、低血糖、便秘、肝機能異常等であった。副作用(785件)の発現後、245件(31.21%)が本剤の投与を中止し、10件(1.27%)が減量した。
| 安全性解析対象症例数 | 6,324 | |
|---|---|---|
| 副作用発現症例数(発現率) | 600(9.49%) | |
| 重度別副作用 発現症例数(発現率) |
非重篤 | 117(1.85%) |
| 重篤 | 508(8.03%) | |
主な副作用(頻度順)
| 副作用の種類 | 発現例数(発現率) |
|---|---|
| 低血糖 | 68(1.08%) |
| 便秘 | 51(0.81%) |
| 肝機能異常 | 32(0.51%) |
| 高血圧 | 21(0.33%) |
| 腎機能障害 | 18(0.28%) |
| 体重増加 | 16(0.25%) |
| 浮動性めまい | 15(0.24%) |
| 血中尿素増加 | 15(0.24%) |
| 脳梗塞 | 13(0.21%) |
| 血中クレアチニン増加 | 13(0.21%) |
死亡は32件が報告され、主な内訳は死亡(原因不明)が6件、急性心不全が2件、脳梗塞が2件であった。投与中止に至った副作用は245件が報告され、主な内訳は便秘18件、低血糖12件、浮動性めまい10件であった。
死亡を含む重篤な副作用(頻度順)
| 副作用の種類 | 発現例数(発現率) |
|---|---|
| 脳梗塞 | 13(0.21%) |
| 死亡 | 6(0.09%) |
| 心筋梗塞 | 5(0.08%) |
| 胃癌、脳出血 | 各4(0.06%) |
| 肺炎、結腸癌 | 各3(0.05%) |
| 虫垂炎、乳癌、食欲減退、狭心症、心房細動、急性心不全、うっ血性心不全、間質性肺疾患、胃腸出血、肝障害 | 各2(0.03%) |
| 壊疽性蜂巣炎、膀胱炎、肺結核、尿路感染、細菌性肺炎、基底細胞癌、胆管細胞癌、肺大細胞癌、 喉頭癌、髄膜腫、膵癌、直腸癌、腎癌、後腹膜癌、肺扁平上皮癌、子宮癌、ワルデンストローム・ マクログロブリン血症、単クローン性免疫グロブリン血症、消化器新生物、腹膜の悪性新生物、 膵神経内分泌腫瘍、再発肝癌、膵管内乳頭粘液性癌、高カリウム血症、低血糖、小脳梗塞、 出血性脳梗塞、正常圧水頭症、パーキンソニズム、ラクナ梗塞、低血糖性意識消失、 血栓性脳梗塞、視力障害、硝子体出血、急性心筋梗塞、不安定狭心症、不整脈、冠動脈硬化症、 第二度房室ブロック、心不全、末梢動脈閉塞性疾患、腸骨動脈閉塞、肺臓炎、十二指腸潰瘍、 胃潰瘍、メレナ、食道静脈瘤出血、大腸ポリープ、下部消化管穿孔、胆管結石、胆管炎、 急性胆管炎、硬化性胆管炎、急性胆嚢炎、肝機能異常、関節痛、関節リウマチ、椎間板突出、 糖尿病性腎症、腎機能障害、慢性腎臓病、急性腎障害、子宮頚部上皮異形成、卵巣嚢胞、 低体温、末梢性浮腫、突然死、廃用症候群、血中クレアチンホスホキナーゼ増加、 血中ブドウ糖増加、心電図ST-T部分異常、事故、過量投与、入院 | 各1(0.02%) |
試験概要
- 対象
- 委受託契約を締結した医療機関において、スイニーを新たに使用する2型糖尿病患者
- 目標症例数
- 3,000例
- 方法
- 電子データ収集システム(EDC)により、中央登録方式で症例を登録し、症例データを収集した。(登録期間:2013年6月から2014年11月に設定した。調査期間:2013年6月から2018年5月に設定した)使用実態下において、本剤の用法及び用量に従い、通常、成人にはスイニー1回100mgを1日2回朝夕に経口投与した。
なお、 効果不十分な場合には、経過を十分に観察しながら1回量を200mgまで増量することができるとし、また用法及び用量に関 連する注意に従い、重度以上の腎機能障害患者では100mg1日1回投与を目安に用量調節することとした。
観察期間は本剤投与開始から3年間(36ヵ月)とし、投与を中止または終了した場合は、その時点で調査終了とした。
[安全性解析対象症例6,324例(調査対象外疾患10例を含む)、有効性解析対象症例6,007例]有害事象の集計については、ICH国際医薬品用語集日本語版MedDRA/J Version 21.0を用いた。 - 調査項目
- 患者背景、本剤の使用状況、併用薬の使用状況、安全性(副作用、臨床検査値)、有効性(HbA1c)、LDL- C、TG 他
- 解析方法
- 安全性解析対象症例について、患者背景因子に基づいて層別解析を実施した。スイニーの効能又は効果および用法及び用量を遵守した症例についての検討を行うため、本剤投与理由が2型糖尿病の症例で、かつ投与開始時の1日投与量が本剤の用法及び用量を下回る50mg使用症例を除いた100mgから400mgの使用症例を日常用量群と定義し、解析を実施した。
HbA1c変化量、LDL-C変化量、TG変化量等について患者背景因子(前治療薬、用量変 更、投与開始時HbAlc、投与開始時LDL-C、投与開始時TGなど)に基づいて層別解析を実施した。
※石田 力 他 : 薬理と治療 49(10) 1589,2021
本調査は、(株)三和化学研究所により行われた。
「禁忌を含む注意事項等情報」等は電子添付をご参照ください
