有効性と安全性
慢性便秘症※患者に対する有効性と安全性を紹介します。
透析患者の有効性と安全性
血液透析実施の慢性便秘症※患者に対する有効性と安全性を紹介します。
作用機序
ラグノスNF経口ゼリーの作用機序についてご紹介します。
※器質的疾患による便秘を除く
01 有効性と安全性
本剤の臨床データパッケージには、被験者の状態に応じた用量調節をして有効性・安全性を評価した試験が含まれています。
そのため、一部国内で承認された用法・用量と異なる試験成績が含まれていますが、承認時評価資料のため紹介します。
臨床成績 国内第Ⅱ/Ⅲ相試験(用量反応試験)
投与第1週における自発排便回数のベースラインからの変化量は、ラグノスNF経口ゼリー48g/日群及び72g/日群で、プラセボ群に対し有意に増加した。
投与第1週の自発排便回数のベースラインからの変化量[主要評価項目]
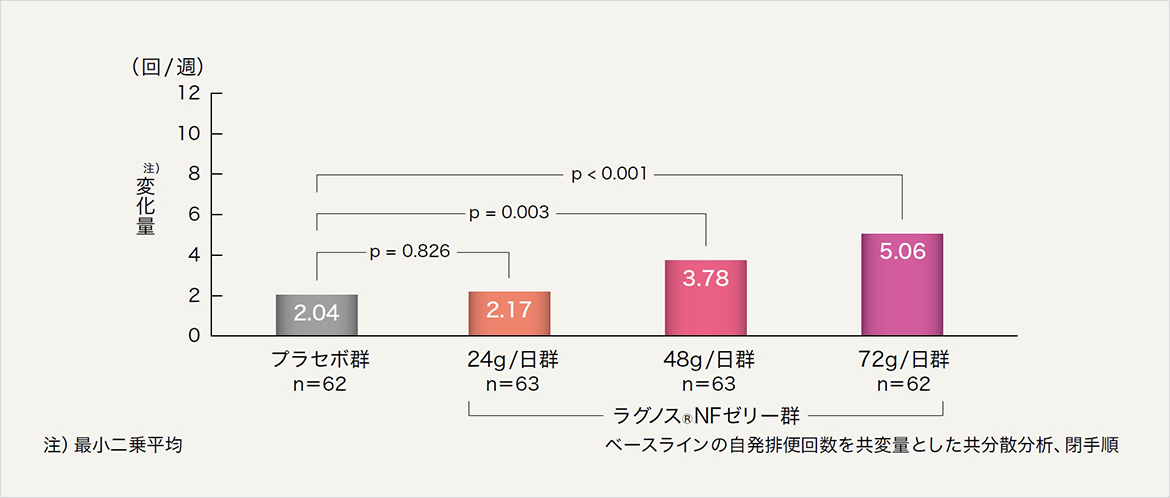
投与第1週の自発排便回数[副次評価項目]
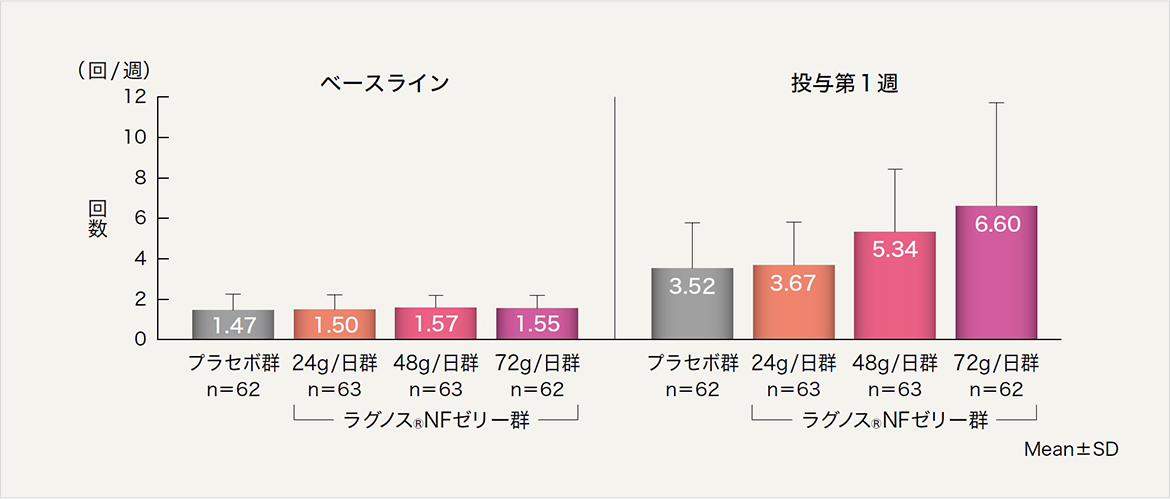
安全性
副作用の発現率は、プラセボ群9.7%(6/62例)、ラグノスNF経口ゼリー24g/日群3.2%(2/63例)、48g/日群6.3%(4/63例)、72g/日群21.0%(13/62例)でした。主な副作用は下痢[72g/日群:9.7%(6/62例)]であり、いずれかの群で2%以上に認められた副作用は下表の通りであった。
本試験において、死亡例を含む重篤な副作用は、いずれの投与群でも認められなかった。
投与中止に至った副作用は、ラグノスNF経口ゼリー24g/日群1例(腹部膨満)、48g/日群1例(蕁麻疹)で認められ、プラセボ群及びラグノスNF経口ゼリー72g/日群では認められなかった。
例数(%)
| 副作用名 | プラセボ群 (n=62) |
ラグノスNF経口ゼリー群 | ||||
|---|---|---|---|---|---|---|
| 24g/日群 (n=63) |
48g/日群 (n=63) |
72g/日群 (n=62) |
全体 (n=188) |
|||
| 副作用発現例数(全体) | 6(9.7) | 2(3.2) | 4(6.3) | 13(21.0) | 19(10.1) | |
| 胃腸障害 | 下痢 | 0(0.0) | 0(0.0) | 0(0.0) | 6(9.7) | 6(3.2) |
| 腹部膨満 | 0(0.0) | 1(1.6) | 1(1.6) | 2(3.2) | 4(2.1) | |
| 腹痛 | 2(3.2) | 0(0.0) | 1(1.6) | 2(3.2) | 3(1.6) | |
| 胃腸音異常 | 0(0.0) | 0(0.0) | 1(1.6) | 2(3.2) | 3(1.6) | |
| 臨床検査 | 総蛋白減少 | 2(3.2) | 0(0.0) | 0(0.0) | 0(0.0) | 0(0.0) |
MedDRA/J version 20.0
試験概要
- 対象
- 慢性便秘症患者※250例
- 方法
- 治験薬として、ラグノスNF経口ゼリー及びプラセボを用意し4群(プラセボ群、ラグノスNF経口ゼリー24g/日群、ラグノスNF経口ゼリー48g/日群、ラグノスNF経口ゼリー72g/日群)に無作為に割り付け、2週間投与した。
- 評価項目
-
- 主要評価項目:投与第1週における自発排便回数(救済薬投与による排便を除く)の変化量
- 副次評価項目:自発排便回数(投与第1週)等
- 安全性(副作用 等)
- 解析計画
-
- 有効性評価の主要解析対象集団は最大解析対象集団(FAS)とした。
- 主要評価項目の主要解析は、各症例で、投与第1週における自発排便回数のベースラインからの変化量を求め、各投与群で要約統計量を算出した。投与群を説明変数、ベースラインの自発排便回数を共変量とした共分散分析モデルを用いてラグノスNF経口ゼリー72g/日群から順番に48g/日群及び24g/日群とプラセボ群との比較を閉手順に従って実施した。
- 副次評価項目の自発排便回数は、投与群ごとに要約統計量を算出した。
※自発排便回数が平均3回/週未満の状態が6ヵ月以上持続している機能性便秘症患者
- 用法・用量(抜粋)
- 慢性便秘症(器質的疾患による便秘を除く):通常、成人には本剤24g(本剤2包)を1日2回経口投与する。症状により適宜増減するが、1日最高用量は72g(本剤6包)までとする。
※承認時評価資料
02 透析患者の有効性と安全性
臨床成績 国内第Ⅲ相試験(血液透析実施の慢性便秘症※患者対象) ※器質的疾患による便秘を除く
いずれの投与期も投与0週と比較して便秘症の重症度が有意に改善した。
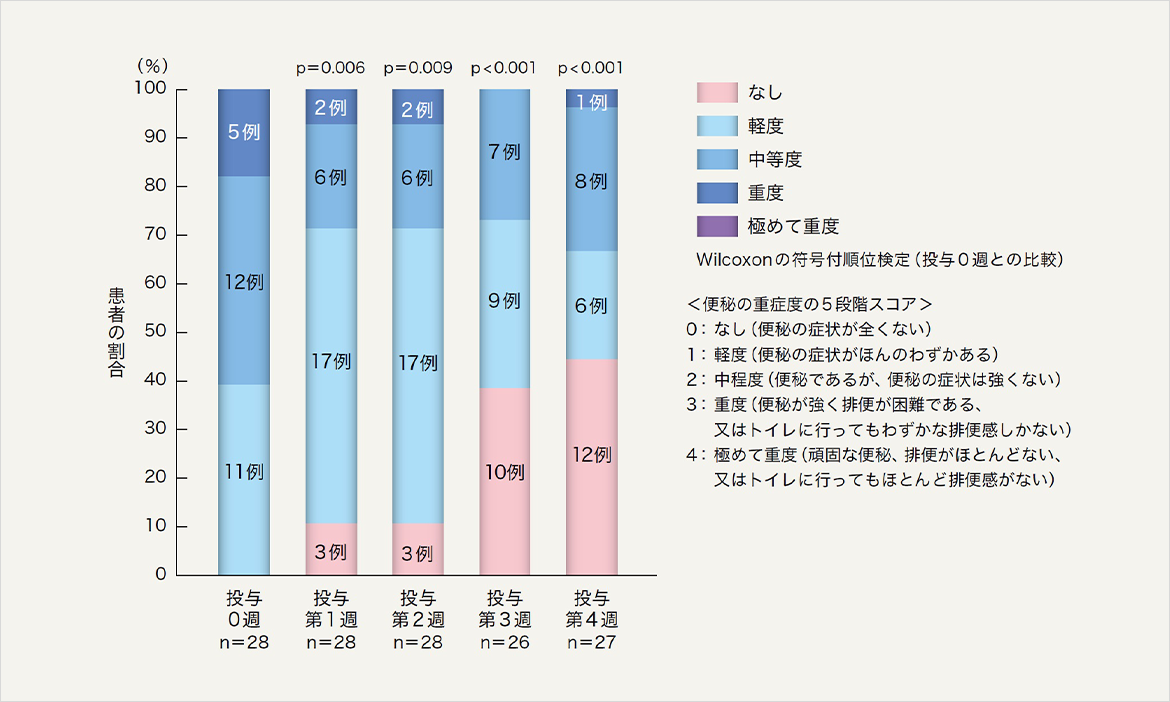
安全性
副作用の発現率は17.9%(5/28例)であり、主な副作用は、下痢10.7%(3/28例)だった。本試験において、死亡例を含む重篤な副作用は認められなかった。投与中止に至った副作用は、1例で下痢が認められた。
例数(%)
| 副作用名 | 発現例数 | |
|---|---|---|
| 副作用発現例数(全体) | 5(17.9) | |
| 胃腸障害 | 下痢 | 3(10.7) |
| 腹部膨満 | 1(3.6) | |
| 鼓腸 | 1(3.6) | |
MedDRA/J version 20.0
試験概要
- 対象
- 血液透析を実施している慢性便秘症患者※28例
- 方法
- ラグノスNF経口ゼリーは、1回12g(1包)1日2回から開始後、被験者の症状に応じて適宜増減し、4週間経口投与した。最大投与量は1回36g(3包)1日72g(6包)までとした。また、血液透析前日の投与を控えることを可とした。
- 評価項目
- 便秘症の重症度評価及びその変化、安全性(副作用 等)等
- 解析計画
-
- 有効性評価の主要解析対象集団は最大解析対象集団(FAS)とした。
- 便秘症の重症度評価及びその変化は、ラグノスNF経口ゼリー投与前と投与後の各評価時点(投与第1週、投与第2週、投与第3週、投与第4週)とのシフトテーブルを作成した。また、ラグノスNF経口ゼリー投与前からの変化に対して、Wilcoxonの符号付順位検定を実施した。
※血液透析を週3回実施している機能性便秘症患者のうち、便秘治療剤を投与しているが治療効果に満足していない患者
用法・用量(抜粋)
慢性便秘症(器質的疾患による便秘を除く):通常、成人には本剤24g(本剤2包)を1日2回経口投与する。症状により適宜増減するが、1日最高用量は72g(本剤6包)までとする。
※承認時評価資料
03 作用機序
作用機序(イメージ図)
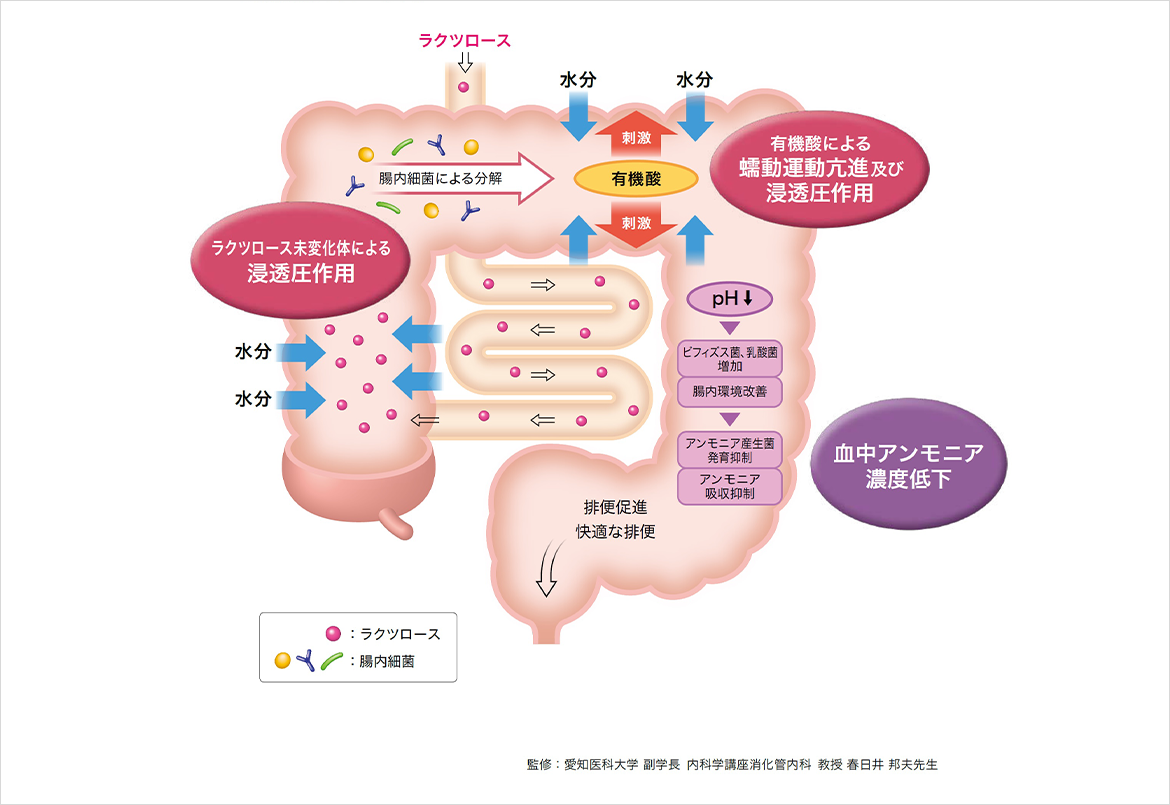
ラクツロースは、小腸で分解・吸収されることなく大腸に達し、ラクツロース未変化体の浸透圧作用により腸内への水の移動を促進する。また、ラクツロース未変化体は、腸内細菌によって分解され、乳酸などの有機酸を産生し、浸透圧を高めるとともに、腸管の蠕動運動を促進し、浸透圧性下剤としての作用を示す。さらに、産生された有機酸によりpHが低下し、ビフィズス菌、乳酸菌の増加及び腸内環境の改善が認められ、アンモニア産生菌の発育を抑制し、アンモニアの吸収を抑制することにより、血中アンモニア濃度の低下作用を示す。
「禁忌を含む使用上の注意」等は電子添文をご参照ください
