測定原理
本品は、LIA法により、子宮頸管粘液中の遊離顆粒球エラスターゼ及びα1プロテアーゼインヒビター〔以下α1P I〕と結合して複合体を形成している顆粒球エラスターゼ(以下、顆粒球エラスターゼ複合体)の両者を合算した量として定量するものです。検体として測定する子宮頸管粘液中には遊離顆粒球エラスターゼと顆粒球エラスターゼ複合体の両者が共存しますが、遊離顆粒球エラスターゼは抽出液中に含まれているα1P Iによって、あらかじめ顆粒球エラスターゼ複合体に変換された後、既に検体中に存在する顆粒球エラスターゼ複合体と共にラテックス粒子に吸着させた2種類の抗ヒト顆粒球エラスターゼ(マウス)モノクローナル抗体(以下、抗体感作ラテックスA、B)が抗原抗体反応を起こし、反応の
進行に伴って抗体感作ラテックスA、Bが凝集し大きな凝集塊を形成します。
この凝集反応を吸光度変化としてとらえたとき、その変化量は検体中の顆粒球エラスターゼ濃度に比例することにより、濃度既知の標準品から検量線を作成し濃度を算出します。
なお、標準品として遊離顆粒球エラスターゼを用いているため、測定値は好中球から放出された顆粒球エラスターゼの量として表されます。
使用上の注意
1. 取扱い上(危険防止)の注意
(1)試料にはHBウイルス等の感染性微生物が存在することがあるので、感染の危険性があるものとして、取扱いには十分注意してください。
(2) 本品中には防腐剤として0.09(W/V)%アジ化ナトリウムが含有されています。誤って目や口に入ったり、皮膚に付着した場合は水で十分に洗い流す等の応急措置を行い、必要があれば医師の手当てを受けてください。
2. 使用上の注意
(1)使用期限の切れた試液は使用しないでください。
(2)試液の開封後はなるべく早く使用し、保存する場合は蓋を閉めて指定の条件で保存してください。
(3)本品中の容器、付属品は他の目的に転用しないでください。
(4)緩衝液及びラテックス試液は、測定前に軽く転倒混和した後、所定の位置に正しくセットしてください。泡立っている場合は泡を取り除いて測定してください。
(5)測定範囲の上限を超える試料は、3倍以上に希釈し、再度測定してください。得られた値に希釈倍数を乗じて測定値を算出します。ださい。
(6)ロットの異なる試液を混ぜ合わせて使用しないでください。
(7)検量線は測定ごとに作成してください。また、検量用試料は、それぞれ2回以上測定してください。
(8)検量用試料は別売品を使用してください。なお使用に際しては別売品の現品説明書を参照してください。
(9)試液は必ず冷蔵 (2~10℃) 保存し、凍結保存は避けてください。
3. 廃棄上の注意
(1)本品中には防腐剤として0.09(W/V)%アジ化ナトリウムを含有しています。アジ化ナトリウムは鉛管、銅管と反応して爆発性の強い金属アジドを生成することがありますので、廃棄する場合には大量の水で洗い流してください。
(2)試料にはHBウイルス等の感染性微生物が存在することがあるので、使用済みの試料、試薬容器、器具等は滅菌、消毒(0.5%次亜塩素酸ナトリウム溶液)、焼却等で処理してください。
(3)試液及び器具などを廃棄する場合には、廃棄物の処理及び清掃に関する法律、水質汚濁防止法等の規定に従って処理してください。
品目仕様等
| 製 品 名 | 内 容 | |
| イノテック・エラスターゼ |
緩衝液(R1) 54mL×1 |
エラスターゼラテックス試液(R2) 10mL×1 |
操作方法
1.試液の調製
緩衝液(R1)、エラスターゼラテックス試液(R2)はそのままご使用ください。
2.試液の安定性
緩衝液(R1)、エラスターゼラテックス試液(R2)共に冷蔵(2~10℃)保存で製造後1年安定です。
3.測定操作法
(1)検体の採取及び抽出方法
子宮膣部を綿球で拭った後、子宮頸管粘液採取用綿棒(以下、綿棒)を子宮頸管内に挿入し、子宮頸管粘液(滲出液)を採取します。抽出液1mLの入った抽出容器に子宮頸管粘液(滲出液)を採取した綿棒を入れてかき混ぜます。次に綿棒を抽出容器に押し当て、綿部に含んでいる抽出液をできるだけ絞り出した後取り除きます。次に、白血球を除去するため抽出容器にフィルターを取り付け、抽出容器を指で押して検体保存用容器に抽出液を滴下し、抽出検体とします。
なお、詳しい検体採取及び抽出方法については、検体採取器具であるエラスペックアシスト(別売)に添付の説明書を参照してください。
(2)検体希釈(測定用検体の調製)
抽出検体は生理食塩水を用いて10倍に希釈し、これを測定用検体とします。なお、検体希釈に際してはガラス容器を使用しないでください。また、測定用検体が測定範囲の上限を越える場合、更に希釈を行って再度測定してください。
(3)測定法 [標準的操作法]〈2ポイント法〉
(下図参照) (反応温度:37℃)
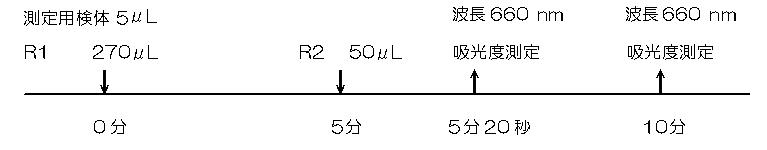
4.検量線 検量線の作成
(1)別売のイノテック・エラスターゼ用顆粒球エラスターゼ標準品を添付文書に従い調製し、上記測定方法に基づいて測定を行い、5点検量線を作成してください。
(2)抽出検体中のエラスターゼ濃度の算出
測定された濃度を10倍して抽出検体濃度としてください。
操作上の注意
(1)測定試料の性質
イ.検体はエラスペック アシストを用いて採取した子宮頸管粘液(滲出液)を使用します。
ロ.検体採取後は、直ちに抽出操作を行い測定します。抽出操作を行った後、直ちに測定しない場合は、8℃保存で3日以内又は-15℃以下に保存した場合は3ヶ月以内に測定してください。
(2)妨害物質等
抽出液中のヘモグロビン(500mg/dL)、総ビリルビン(50mg/dL)は影響を与えません。
(3)その他
イ.試液は必ず冷蔵保存 (2~10℃) し、凍結保存は避けてください。
ロ.各種自動分析装置への適応例については、別途資料をご請求ください。
性能
1.感度
自社施設において本品を用い、1000ng/mLの顆粒球エラスターゼ標準液を試料として操作したところ、吸光度差は0.060~0.150/minの範囲内でした。
2.正確性
自社施設において本品を用い、下記の2種類の管理検体を5回測定したところ、結果は下記のとおりでした。
| 管理検体1 (1.51μg/mL) |
管理検体2 (5.18μg /mL) |
|
| 測定値(μg/mL) | 1.53~1.62 | 5.02~5.04 |
| 表示値に対する収率(%) | 101.3~107.3 | 96.9~97.3 |
3.同時再現性
自社施設において本品を用い、下記の2種類の検体を5回同時に測定したところ、結果は下記のとおりでした。
| 管理検体1 | 管理検体2 | |
| 平均値(μg/mL) | 1.56 | 5.01 |
| 標準誤差 | 0.03 | 0.02 |
| C.V. (%) | 2.12 | 0.50 |
4検出範囲
生理食塩水で10倍希釈された測定用検体中の顆粒球エラスターゼの本品による測定範囲は5.0~1000ng/mLです。
特長
1. 2種類のモノクロナール抗体を使用しラテックス凝集免疫比濁法を測定原理とした試薬です。
2.各種汎用自動分析装置への適応が可能です。
3.試液調製が不要です。
4.試料の前処理 (試料の希釈) が不要です。
